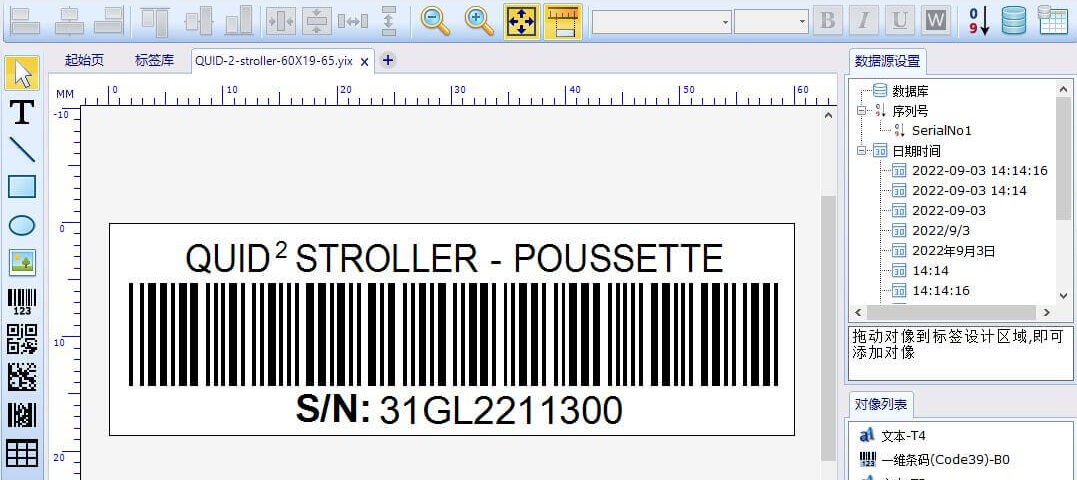
UDI 标签增强设备可追溯性的五种方式
过去几年,医疗器械制造商一直在为其产品推出唯一器械标识符 (UDI),以符合 FDA 的 UDI 标签要求。今年 9 月 24 日,UDI 规则将达到其第四个里程碑,届时将要求额外的设备带有永久性标记或标签。
UDI 计划的启动是为了帮助提高医疗器械的可追溯性和召回率,但也有其他好处。通过更好的设备跟踪,医院可以提高内部效率、减少医疗错误并更好地优化设备的使用。
从 2014 年到 2016 年,各种设备制造商被要求实施 UDI 标签或提交设备数据以填充设备数据库(全球 UDI 数据库,或 GUDID),该数据库充当数据的中央存储库。
UDI 标签如何使医疗保健提供者受益
随着这些设备现在在医院和其他设施中使用,提供者和其他医疗保健利益相关者可以潜在地利用 UDI 来实现许多好处:
- 减少医疗错误:通过将设备数据与患者识别和其他数据收集过程联系起来,供应商可以确保为正确的患者发放正确的医疗设备。在手术室中,UDI 可以帮助在手术前后自动进行库存盘点,以确保设备随时可用。
- 增强的设备分析:UDI 可以提供一种标准方法来记录电子健康记录和临床信息系统中的设备使用情况。UDI 标签还可以帮助创建更强大的上市后跟踪系统,该系统可用于支持新设备的批准或许可或当前设备的新用途。
- 更准确的设备报告:可以更准确地报告不良事件并链接到特定设备,从而可以更快地发现潜在问题。
- 减少假冒/转移:医疗设备非常有价值,而供应链中充斥着欺诈行为。UDI 标签可以确保到达的设备不是假冒产品,还可以帮助识别被盗设备,然后在售后市场重新出售。
- 改进召回:拥有标准标识符还将帮助制造商、分销商和医疗机构更有效地管理医疗器械召回。可以跟踪特定设备的使用点,从而使召回更有针对性和有效性。

UDI 里程碑
随着最后期限的临近,将要求更多的医疗设备带有 UDI 标志或标签。即将到来的 9 月 24 日截止日期将包括:
- 需要使用 UDI 标记的 II 类设备如果要多次使用,则必须在设备本身上带有永久性 UDI 标记。
- I 类器械和非分类器械的标签和包装必须带有 UDI。
- 所有设备(包括免于 UDI 的设备)标签上的日期必须按照 FDA 要求进行格式化
- 属于 UDI 要求的 I 类和未分类设备的数据必须提交给 GUDID;I 类独立软件也必须提供 UDI。
UDI 的下一个重要里程碑是 2020 年 9 月,届时所有符合要求的 I 类设备或未分类的设备都必须带有 UDI 作为永久标记,如果该设备将被多次使用。
条码标签软件可以帮助确保您的标签符合 UDI 标准。易标签软件已被医疗设备制造商使用。使用合适的标签软件,您可以轻松地自动化和管理 UDI 标签要求。
需要帮助实施 UDI 标签要求的公司,或希望更好地利用带有 UDI 标记的设备的供应商,可以联系联印通以获取有关其标签和直接标记需求的帮助。